甲烷的用途很廣泛。
(1)已知:
2NO2(g ) N2O4(g) △H= -56.9kJ·mol -1
N2O4(g) △H= -56.9kJ·mol -1
H2 O(g)= H2O(l) △H= -44.0kJ·mol -1
CH4(g)+N2O4 (g)= N2(g)+2H2O(l)+CO2 (g) △H=-898.1kJ·mol -1
則 CH4 (g)催化還原NO2 (g)生成 N2(g)和H2O(g)的熱化學方程式為_____________________�。
(2)一定條件下,發(fā)生2NO(g)+2CO(g) N2(g) +2CO2(g) △H<0�。在不同時間c(NO)與c(CO)如下表所示:
N2(g) +2CO2(g) △H<0�。在不同時間c(NO)與c(CO)如下表所示:
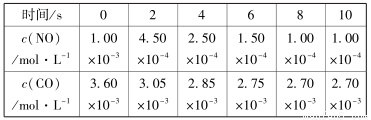
①該溫度下,該反應(yīng)的平衡常數(shù)表達式為K =_____________________����;
②計算前4秒內(nèi)氮氣的平均反應(yīng)速率為____________________���;
③下列選項中,不能說明上述反應(yīng)已達平衡的是( )
A.2v正(NO)= v逆(N2 )
B.容器中氣體的平均分子量不隨時間而變化
C.容器中氣體的密度不隨時間而變化
D.容器中CO的質(zhì)量不再發(fā)生變化
E. 容器中氣體的總壓強不隨時間而變化
(3)CH4燃料電池原理如圖所示
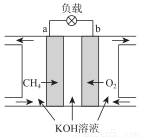
①該燃料電池的正極為_______________(填“a”或“b”)����。該電池負極的電極反應(yīng)式為_____________;
②放電一段時間后�����,電解質(zhì)溶液的pH___________(填“增大”�、“減小”或“不變”)。